Los gases ideales son gases teóricos formados por una serie de partículas precisas y exactas con desplazamiento aleatorio que no interactúan entre sí.
Categoría: Guía de Estudios
Aleaciones
Las aleaciones son mezclas homogéneas formadas generalmente por dos o más metales, aunque es posible también la aleación entre metales y no metales; obtenida por fusión y solidificación de estos.
Masa atómica, masa molecular y masa molar.
La masa atómica, molecular y molar son unidades de gran importancia para los cálculos estequiométricos. Los cálculos estequiométricos son aquellos que nos permiten conocer las relaciones fijas de combinación que hay entre las sustancias en las reacciones químicas balanceadas.

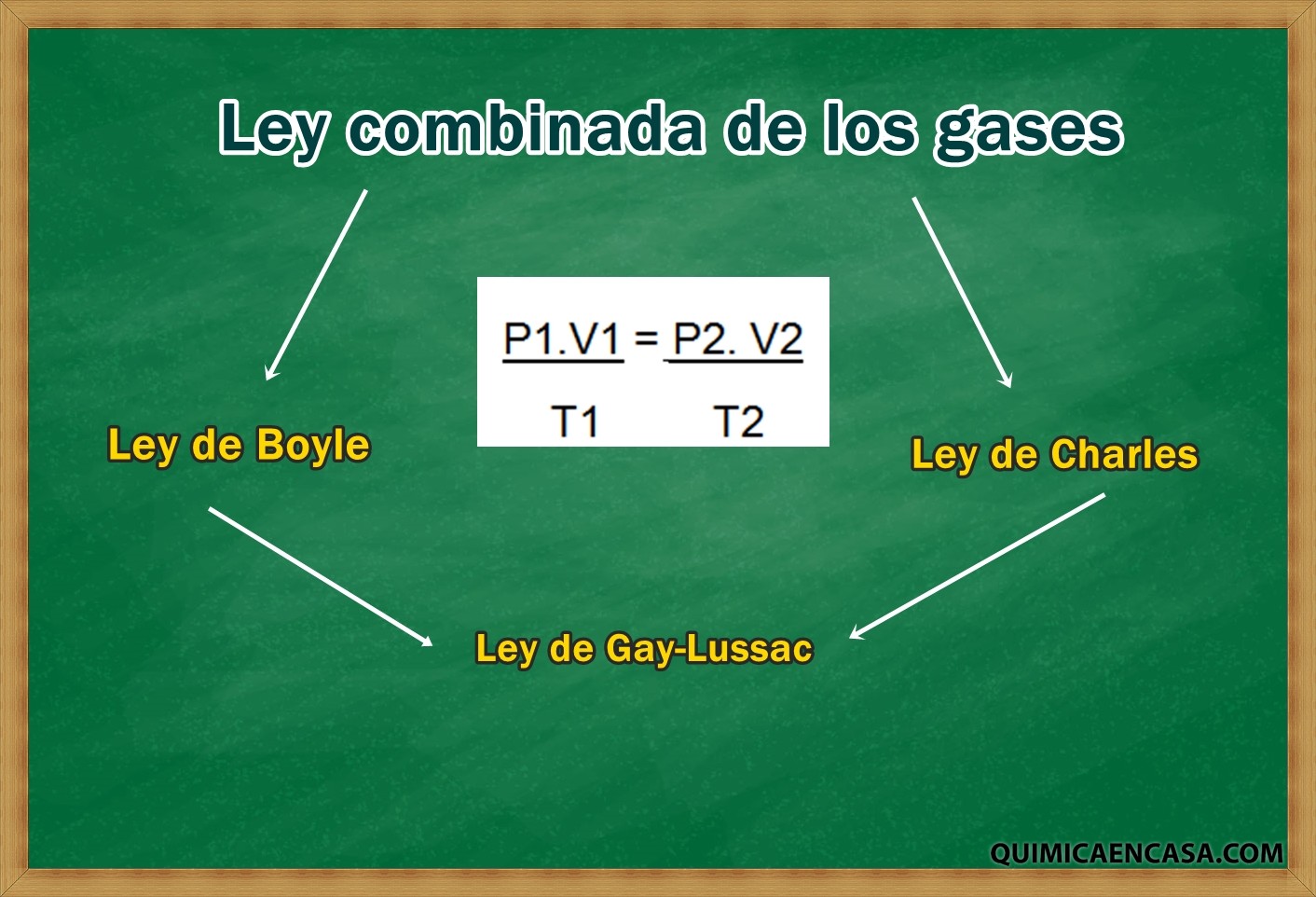
Ley combinada de los gases. Ejercicios Resueltos.
La ley combinada de los gases es aquella que unifica las leyes de Charles, la ley de Gay-Lussac y la ley de Boyle. En esta ley se relaciona las variables de presión, volumen y temperatura de una cantidad fija de un gas.
Leer más…«Ley combinada de los gases. Ejercicios Resueltos.»
Ley de Gay-Lussac
La ley de Gay-Lusacc es una de las leyes de los gases. Esta establece que la presión de un volumen fijo de un gas, es directamente proporcional a su temperatura.
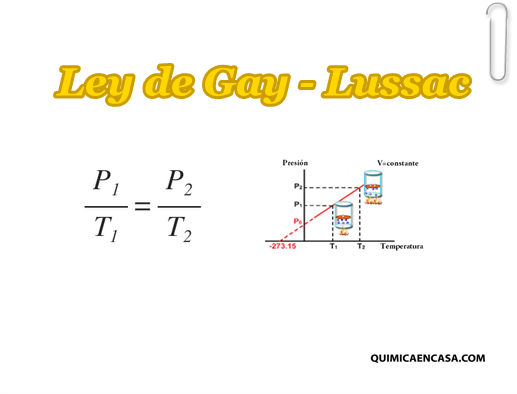
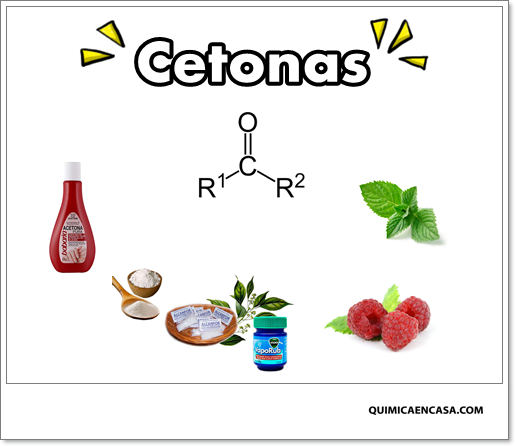
Cetonas. Ejercicios Resueltos.
Las cetonas son compuestos orgánicos del grupo de los carbonilos (un carbono enlazado mediante un doble enlace a un oxígeno), que se distingue de los aldehídos, en el hecho de que los átomos de carbono de estos están doblemente sustituidos por grupos R y los aldehídos solo por un grupo R y un hidrógeno.
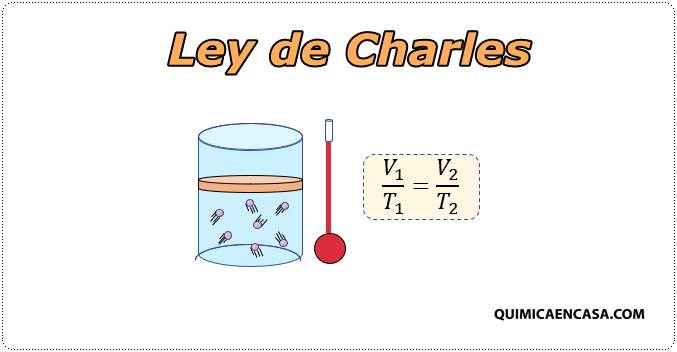
Ley de Charles
La ley de Charles es una de las leyes de los gases. Esta relaciona el volumen y la temperatura de una cantidad especifica de gas ideal, a una presión constante, a través de una constante de proporcionalidad directa.
Ley de Boyle-Mariotte
Robert Boyle fue un filósofo natural, químico, físico, inventor y teólogo cristiano. Además es considerado como el primer químico moderno y por consiguiente, uno de los fundadores de la química moderna y por formular la ley de Boyle.
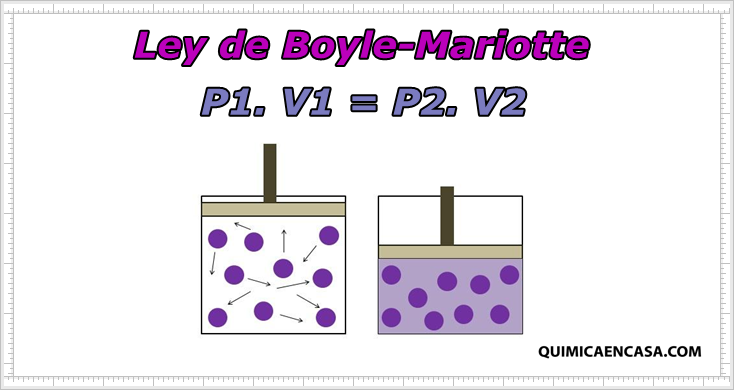
Por su parte, Edme Mariotte fue un abad, físico y químico francés. Estudió la compresión de los gases y llegó a descubrir la ley hoy conocida como ley de Boyle-Mariotte.
Ambos científicos (Boyle y Mariotte), de forma independiente, llegaron a la misma ley. Cabe destacar que Boyle en sus escritos no especificó que la temperatura debía ser constante para que la ley fuese válida; probablemente realizó sus experimentos y lo daría por hecho. No obstante, Mariotte si especificó esta constancia
Ley de las proporciones múltiples
La ley de las proporciones múltiples, señala que cuando dos elementos se unen formando dos o más sustancias compuestas, la masa de un elemento permanece fijo, mientras que la masa del otro elemento varía en una relación de número enteros sencillos.

Composición Centesimal. Ejercicios Resueltos
Se entiende por composición centesimal de una sustancia, los valores en términos de porcentaje de cada uno de los elementos que la constituyen. Se obtiene por análisis gravimétrico y conociendo las masas atómicas de los compuestos puede determinarse su fórmula mínima o molecular.




