En química, las moléculas no son planas, pero el papel y las pantallas sí lo son. Para resolver este dilema, los químicos inventaron diferentes «proyecciones». Cada una tiene un propósito específico: algunas sirven para ver rotaciones, otras para azúcares y otras para ciclos.
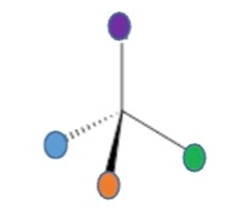
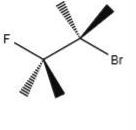
1. Proyección de Cuña y Enlace (3D Estándar)
Es la forma más común de representar la estereoquímica.
- Características: Usa líneas normales para enlaces en el plano, cuñas rellenas para lo que sale hacia ti y cuñas discontinuas para lo que se aleja.
- Uso: Dibujo general de cualquier molécula orgánica.
2. Proyección de Newman
Imagina que miras la molécula directamente a lo largo de un enlace carbono-carbono.
- Características: El átomo delantero es un punto y el trasero es un círculo.
- Uso: Es perfecta para estudiar la estabilidad de los confórmeros (eclipsada vs. alternada) y las interacciones de torsión.

Leer más…«El Arte de Dibujar Moléculas: Guía de Proyecciones Orgánicas»