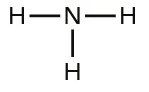
En el mundo de la química, a menudo dibujamos moléculas y damos por hecho que los electrones se reparten de forma equitativa. Sin embargo, para entender cómo reaccionan las sustancias, necesitamos llevar una «contabilidad electrónica». Aquí es donde entra la Carga Formal.
¿Qué es la Carga Formal?
La carga formal es una herramienta que usamos los químicos para saber si un átomo dentro de una molécula tiene más o menos electrones de los que debería tener en su estado natural. No es una carga real como la de un ion, sino una forma de evaluar la estabilidad de nuestras estructuras de Lewis.
La Fórmula Maestra
Para calcularla, solo necesitas esta sencilla fórmula:
Carga Formal = (e– de valencia) – (e– de enlace) ÷ 2 – (e– libres)
Tip para principiantes: Si no quieres dividir, simplemente cuenta los puntos (electrones libres) y las rayitas (enlaces) que tocan al átomo:
C.F. = Valencia – Rayitas – Puntos
Leer más…«¿Quién tiene los electrones? Una guía sencilla sobre Cargas Formales»