Los estados de oxidación son los números que se le asignan al átomo de un elemento o de compuestos para poder determinar el desplazamiento de los electrones en una reacción química, siguiendo un conjunto de reglas que se especificarán más adelante. Normalmente el estado de oxidación es un número entero pero puede ser fraccionado, tal como +8/3 para el hierro en la magnetita (Fe3O4).

También pueden ser positivos o negativos y tener un valor de cero. El mayor estado de oxidación conocido es +8 para los tetraóxidos de rutenio, xenón, osmio, iridio, hassio y algunos compuestos complejos de plutonio, mientras que el menor estado de oxidación conocido es -4 para algunos elementos del grupo del carbono (elementos del grupo 14).
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de míReglas generales para determinar el estado de oxidación a un átomo de un elemento o compuesto.
- En el estado elemental o no combinado, los átomos tienen un estado de oxidación de cero.
- En compuestos, el estado de oxidación del flúor es siempre -1.
- En compuestos, los elementos del grupo 1 tienen un estado de oxidación de +1.
- En compuestos, los elementos del grupo 2 tienen un estado de oxidación de +2.
- En compuestos, el hidrógeno tiene generalmente un estado de oxidación de +1 (en ácidos), excepto en los hidruros, donde el estado de oxidación es -1.
- En compuestos, el oxígeno recibe generalmente el estado de oxidación de -2, excepto los peróxidos donde el oxígeno tiene un estado de oxidación de -1.
- En las especies neutras, la suma de los estados de oxidación de cada átomo multiplicado por el número de cada uno debe dar un total de cero.
- En las especies iónicas, la suma de los estados de oxidación de cada átomo multiplicado por el número de cada uno, debe dar en total la carga del ion.
Ejercicios
¿Cuál es el estado de oxidación del fósforo en el H3PO4?
Este compuesto es un ácido oxácido, por lo tanto el hidrógeno trabaja con estado de oxidación (valencia) igual a +1 y el oxígeno con valencia igual a -2. Nuestra incógnita es el fósforo, el cual posee los siguientes estado de oxidación: +/- 3,4,5. Entonces debemos hacer el cálculo para saber con cuál de sus estados de oxidación está trabajando en dicho compuesto.
Para el cálculo se coloca arriba de cada elemento los estados de oxidación que ostenta y en el caso del fósforo colocamos una X para indicar que es la incógnita, de la siguiente manera:
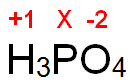
Ahora, el paso siguiente es multiplicar los subíndices de cada elemento por los estados de oxidación, quedando una ecuación matemática, la cual igualaremos a cero ya que este compuesto (ácido fosfórico) es una especie neutra.
3. (+1)+X+ 4.(-2) = 0
3+ X-8 = 0
X= 8-3
X= 5
Entonces, +5 es el estado de oxidación del fósforo en el ácido fosfórico.
¿Cuál es el estado de oxidación del azufre en el ion sulfato SO4= ?
En este caso procedo de igual manera como expliqué anteriormente, con la diferencia de que al no ser una especie neutra sino iónica, la ecuación matemática se debe igualar al estado de oxidación que presente dicho ion, que en este caso es -2.
En este ejercicio se pide calcular el estado de oxidación del azufre en el ion sulfato. El azufre posee los siguientes estados de oxidación:-2,+2,+4,+6; por lo tanto, haremos el cálculo para saber con cual estado de oxidación está trabajando en el ion sulfato.
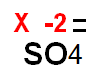
1.(X) + 4. (-2) = -2
X-8 = -2
X= 8-2
X=6
Entonces, +6 es el estado de oxidación del azufre en el ion sulfato.
¿Cuál es el estado de oxidación del carbono en el Fe2(CO3)3 ?
Como sabemos que la incógnita es el carbono, debemos conocer los estados de oxidación de los otros elementos que conforman al compuesto. El oxígeno presenta estado de oxidación -2 y el hierro puede ser +2 o +3. Ahora bien, si observamos atentamente el compuesto, podremos notar que el hierro está trabajando en su estado de oxidación más alto (+3). Recordemos que las valencias se intercambian en los compuestos.
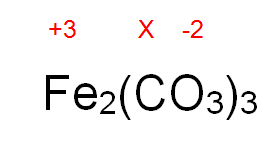
2. (+3) + 3.1.(X) + 3.3. (-2) = 0
+6+3X-18 = 0
·3X = 18-6
3X = 12
X= 12/3
X=4
Entonces, +4 es el estado de oxidación del carbono en el carbonato de hierro (III).

