Cada elemento químico tiene una “firma luminosa” única. Cuando un átomo absorbe o emite luz, lo hace en longitudes de onda específicas que funcionan como un código de barras. La espectroscopía de absorción y emisión atómica aprovecha este fenómeno para identificar elementos y medir sus concentraciones con una precisión extraordinaria. Es una técnica fundamental en química analítica, astronomía, medicina y control de calidad industrial.
¿Qué es la espectroscopía atómica?
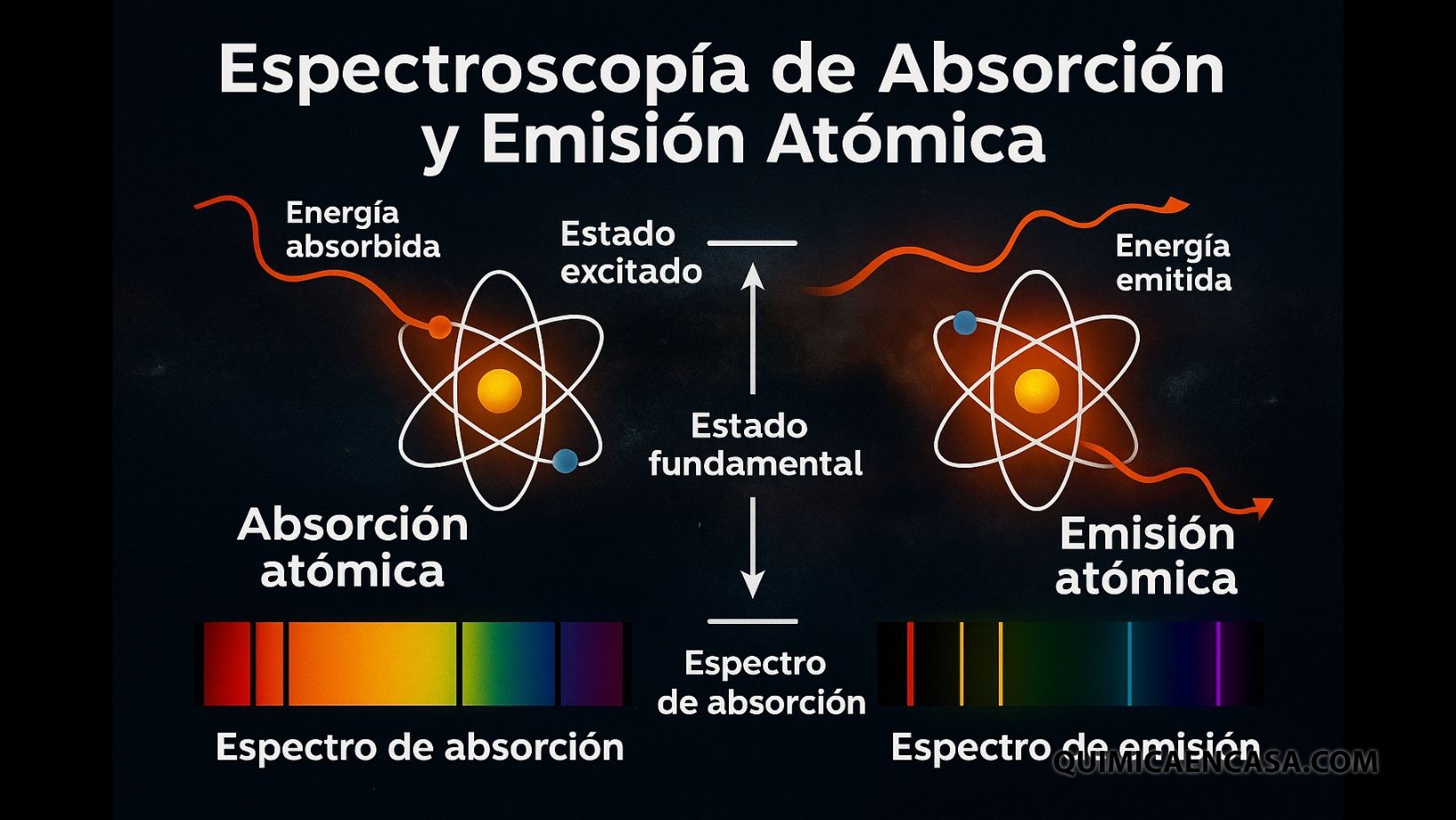
Es el estudio de cómo los átomos interactúan con la luz.
Dependiendo del proceso, puede ser:
- Absorción atómica: el átomo absorbe energía (luz) y sus electrones saltan a niveles superiores.
- Emisión atómica: el átomo libera energía en forma de luz cuando los electrones regresan a niveles inferiores.
Cada transición electrónica produce o absorbe longitudes de onda específicas, creando un espectro característico.
Leer más…«La espectroscopía de absorción y emisión atómica: cómo los átomos revelan su identidad»