El balanceo de ecuaciones redox tiene su “truco” y no es tan sencillo como el balanceo por tanteo, por eso hoy en química en casa te enseñaremos los pasos para el balanceo redox siguiendo el método ión-electrón tanto para disoluciones ácidos como para disoluciones básicas.
A continuación se enumeran los pasos:
- Escribe una ecuación esquemática que incluya aquellos reactivos y productos que contenga los elementos que sufren una variación del estado de oxidación.
Construcción de las semireacciones
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de mí- Seguidamente, se escribe nuevamente una ecuación esquemática parcial para el agente oxidante con el elemento que sufre una reducción en el estado de oxidación en cada miembro de la ecuación. El elemento no deberá escribirse como un átomo libre o ión a no ser que existe de una especie real molecular o iónica.
- Realiza otra ecuación esquemática parcial para el agente reductor, con el elemento que sufre un aumento en el estado de oxidación de cada miembro.
Este paso es muy importante, ya que debemos igualar cada ecuación parcial en cuanto al número de átomos de cada elemento hay.
Balanceo de hidrógenos y oxígenos ( reacciones neutras y/o ácidas)
En disoluciones ácidas o neutras, debe añadirse H2O y H+ para conseguir la igualdad de átomos de oxígeno e hidrógeno. Los átomos de oxígeno se igualan primero. Por ser cada átomo de oxígeno en exceso en un miembro de la ecuación se asegura su igualación agregando agua en el otro miembro. Después se utiliza iones hidrón (H+) para igualar los hidrógenos.
Balanceo de hidrógenos y oxígenos (reacciones básicas)
Ahora bien, si la ecuación es básica, se emplea el ion hidroxilo (OH–). En este caso, por cada oxígeno en exceso en un miembro de una ecuación se asegura su igualación agregando una molécula de agua en el otro miembro. Si hay en exceso hidrógeno y oxígeno en el mismo miembro de la ecuación, se escribe un OH– en el otro miembro por cada pareja de exceso de oxigeno e hidrogeno.
Si algún elemento que sufre un cambio en el estado de oxidación se acompleja en uno de sus estados con algún otro elemento, debe igualarse los grupos que se acomplejan con una especie de este elemento en el mismo estado de oxidación con que se encuentra en el complejo.
Balanceo e igualación de cargas
Ahora es necesario igualar cada ecuación parcial en cuanto al número de carga, esto se realiza agregando electrones en el primer o segundo miembro de la ecuación. En esta entrada te explico detalladamente como se realiza: Balanceo de ecuaciones redox: Método del número de oxidación
Multiplica cada ecuación parcial por un número escogido de modo que el número total de electrones perdidos por el agente reductor sea igual al número de electrones ganados por el agente oxidante.
Sumar las ecuaciones parciales resultantes del paso 7. Los términos comunes de ambos miembros se anulan. Los electrones deben anularse.
Transformar la reacción iónica a molecular
Este paso suele ser opcional, dependiendo del tipo de ecuación que se nos presente. En los casos, donde intervenga la masa de los reactantes o productos, se debe transformar la ecuación iónica del paso anterior, en una reacción molecular. Este paso se realiza agregando en cada miembro de la ecuación, números iguales de los iones que no sufren transferencia de electrones pero que están presentes junto a los componentes reactivos en las sustancias químicas neutras. Algunas parejas adecuadas de iones pueden unirse para generar una fórmula molecular.
Comprobación de la ecuación
Realizar la comprobación de la ecuación final contando el número de átomos de cada elemento en ambos miembros de la ecuación y calculando la carga neta en cada uno de ellos.
Balancee las siguientes ecuaciones redox utilizando el método ión-electrón
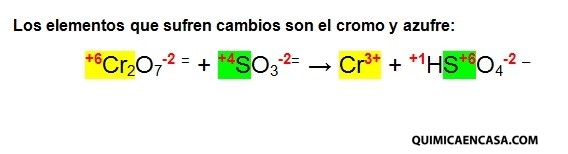
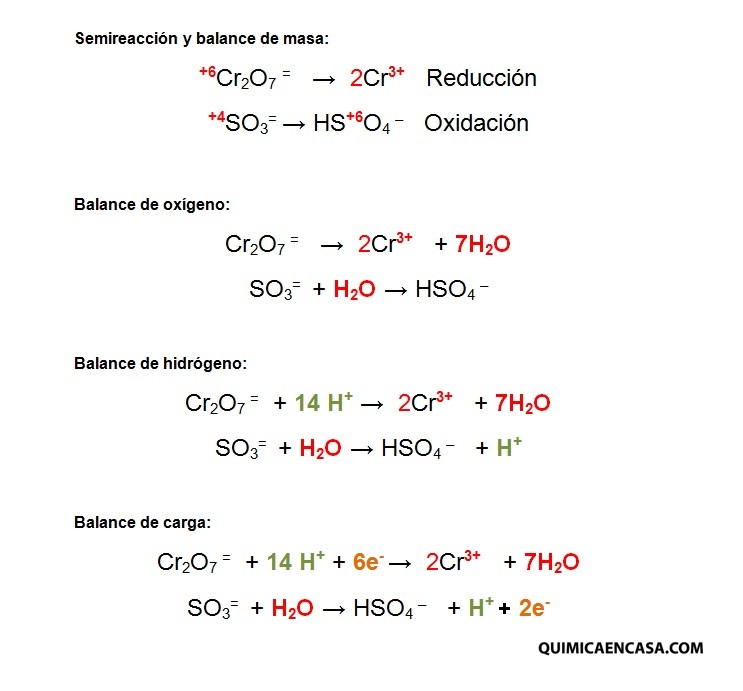
Medio ácido
Cr2O7= + H2SO3 → Cr3+ + HSO4–
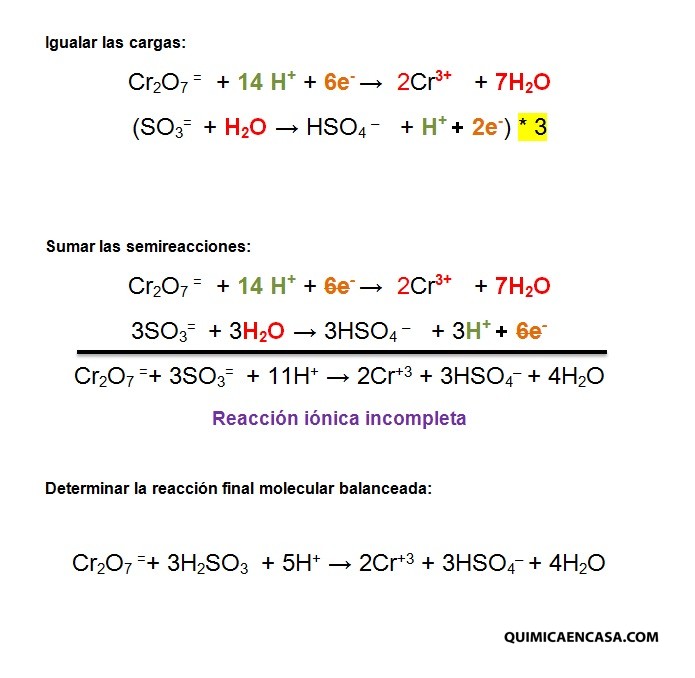
Medio básico
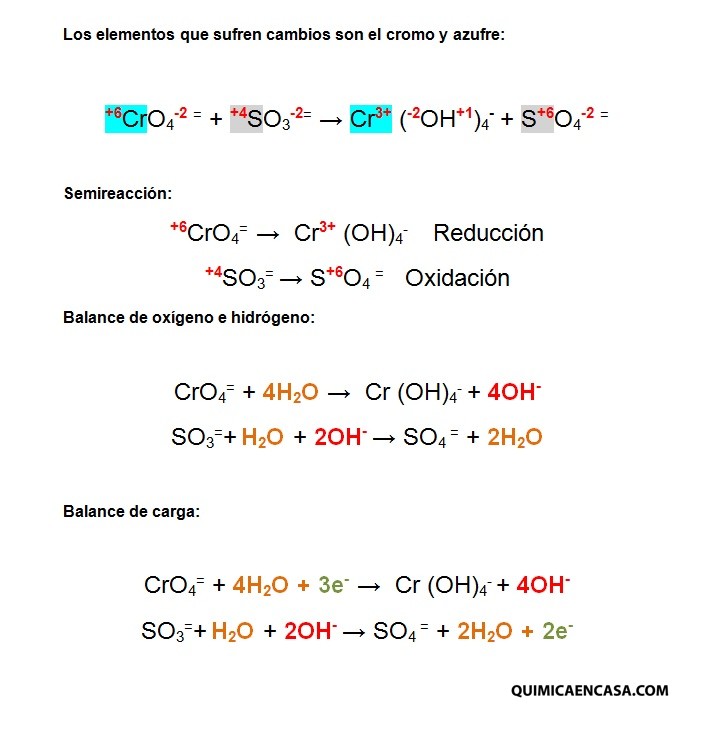
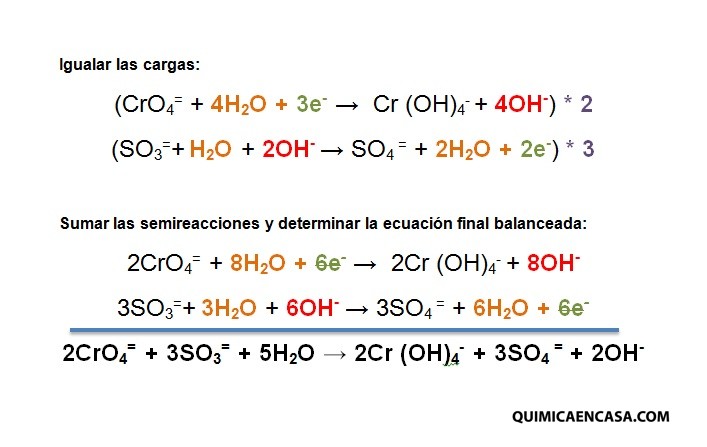
CrO4= + SO3= → Cr (OH) 4– + SO4=