La organización molecular de un sólido nos determina las propiedades del mismo. Es por eso que tenemos dos tipos de sólidos: los amorfos y los cristalinos. Pero, ¿Qué es un sólido cristalino y un sólido amorfo? ¿Cómo podemos diferenciarlos? Sigue leyendo y te explicaremos de qué va cada uno.
Sólidos amorfos
Son aquellos sólidos que tienen una estructura molecular irregular, es decir sus átomos y moléculas están dispuestas de manera tal que no se forma una estructura ordenada y definida. Dicha estructura molecular es similar a la que presentan los líquidos, con la diferencia de que este presenta mayor fuerza de cohesión.
Una propiedad destacada que presenta los sólidos amorfos es que son isotrópicos. Esto significa que ellos son independientes de la dirección en la cual son medidos, debido a su irregularidad.
Algunos ejemplos de sólidos amorfos sería: los plásticos, vidrio, mantequilla, goma, gel, caucho, polímeros, entre otros.
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de mí
Sólidos cristalinos
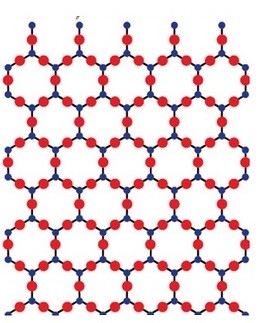
Los sólidos cristalinos son aquellos que poseen átomos o moléculas que están dispuestos de manera tal que forman una estructura completamente definida y ordenada. Dichas superficies definidas, lisas y planas son llamadas caras, las cuales están compuestas por una serie de agrupaciones ordenadas de átomos con ángulos definidos, formando estructuras que siguen un modelo característico para una categoría de red cristalina, ya sea de forma hexagonal, cúbica, romboédrica, triclínica, etc.
A diferencia de los sólidos amorfos, los sólidos cristalinos son anisotrópicos, esto quiere decir que sus propiedades eléctricas y mecánicas obedecen en general de la dirección en que se miden. La anisotropía de los cristales es una propiedad macroscópica muy importante porque proporciona una eficaz indicación de la existencia de una red atómica ordenada.
Algunos ejemplos de sólidos cristalinos son: el grafito, diamante, hierro, cloruro de sodio, hielo, hielo seco, entre otros.
Diferencias
A continuación se presenta un cuadro comparativo con algunas de las diferencias más destacadas entre los sólidos amorfos y sólidos cristalinos.
| Sólidos amorfos | Sólidos cristalinos |
| Disposición de átomos indefinida | Disposición de átomos definida |
| Son menos rígidos | Son más rígidos |
| Manifiestan propiedades isotrópicas | Presentan propiedades anisotrópicas |
| Geometría irregular | Geometría regular |
| Poseen fuerzas intermoleculares no uniformes | Muestran fuerzas intermoleculares uniformes entre ellos |

