El grupo 17 de la tabla periódica es también conocido como halógenos. El término halógeno procede del griego y significa formador de sales. Dicho término, surge por la propiedad que posee cada uno de los halógenos de formar, con el sodio, una sal similar a la sal común (cloruro de sodio).

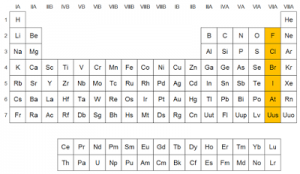
El grupo 17 está formado por los siguientes elementos: flúor (F), cloro (Cl), bromo (Br), yodo (I), ástato (At) y tennessine (Ts).
Estos elementos se hallan en estado elemental formando moléculas diatómicas, aunque aún no está comprobado con el ástato), las cuales son químicamente activas y de fórmula X2. Posee la siguiente distribución electrónica: s2p5. Para llenar por completo su último nivel energético se necesita de un electrón más, por lo que poseen disposición a formar un ion mononegativo llamado haluro (X–).
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de mí
Propiedades físicas.
Son elementos no metálicos.
El carácter metálico aumenta según se desciende en el grupo, es decir, a medida que aumenta el número atómico, por lo tanto, el yodo posee brillo metálico.
Los halógenos se presentan en moléculas diatómicas y sus átomos se mantienen unidos por enlace covalente simple y la fuerza de dicho enlace disminuye al descender en el grupo.
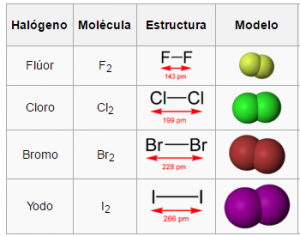
Los puntos de fusión y ebullición aumentan al descender en el grupo.
Estos elementos, a temperatura ambiente, se hallan en los tres estados de la materia: en estado sólido el iodo y ástato, en estado líquido: bromo y en estado gaseoso el flúor y cloro.
El flúor es un gas de color amarillo claro, levemente más pesado que el aire, corrosivo y de olor fuerte e irritante.
El cloro es un gas amarillo verdoso de olor irritante y fuerte.
El bromo es un líquido de color rojo oscuro, muchísimo más denso que el agua, que fácilmente se evapora originando un vapor rojizo venenoso.
El yodo es un sólido cristalino de color negro y brillante, que sublima originando un vapor violeta bastante denso, venenoso y con un olor fuerte e irritante semejante al cloro.
El ástato es muy raro, debido a que es producto intermedio de unas series de desintegración radiactiva.

Propiedades químicas
Los halógenos poseen 7 electrones en su capa más externa, lo que les proporciona un número de oxidación de -1, siendo considerablemente reactivos. Dicha reactividad disminuye según aumenta el número atómico.
De igual manera, también exhiben los estados de oxidación +1, +3, +5, +7, con excepción del flúor, el cual es el elemento más reactivo y más electronegativo del grupo y de la tabla periódica.
Se disuelven en agua y reaccionan parcialmente con ella, a excepción del flúor que la oxida.
Reaccionan con el oxígeno produciendo óxidos inestables. Dicha reactividad disminuye a medida que se desciende en el grupo.
Reaccionan con el hidrógeno para originar haluros de hidrógeno, los cuales se disuelven en agua, generando los ácidos hidrácidos. El ácido más fuerte es el yoduro de hidrógeno (HI).

Reaccionan con algunos metales formando haluros metálicos, casi todos ellos iónicos.

Usos y aplicaciones de los elementos del grupo 17
Flúor
El elemento cabecera de grupo posee una gran cantidad de aplicaciones en la industria y cotidianidad. Por ejemplo, es usado para elaborar televisores de pantallas plasma, pantallas planas y sistemas microelectromecánicos.

En medicina es utilizado el flúor en ciertos antibióticos que intervienen en contra de una extensa gama de bacterias. Estos compuestos de flúor también son empleados en la preparación de anestésicos.
El flúor-18 es el radionúclido del flúor con el mayor período de semidesintegración: 109,771 minutos. Por lo cual es utilizado comercialmente como fuente de positrones. De hecho su aplicación primordial es en la obtención de fluorodesoxiglucosa radiofarmacéutica para su uso en la técnica clínica de tomografía por emisión de positrones.
Ciertos compuestos de flúor como fluoruro de sodio, fluoruro estañoso y monofluorofosfato de sodio, son agregados a las cremas dentales para prevenir las caries.

El fluoruro de sodio también es empleado como complemento de soldaduras, metalurgia, en la preparación de raticidas, en la industria del vidrio, en la fluoración del agua, entre otros.
El flúor es utilizado para obtener ácido fluorhídrico, el cual es empleado para grabar vidrio, habitualmente en las bombillas.
De igual manera, el flúor se usa para la elaboración de halones. Los halones son hidrocarburos halogenados utilizados como agentes extinguidores de incendios, como por ejemplo, el freón.
A partir del hexafluoruro de uranio se puede obtener uranio puro. Debido a que sus moléculas presentan una gran masa, es posible usar el centrifugado para separar los isótopos U-235 y U-238, adquiriéndose uranio puro.
El flúor es extensamente empleado en la producción de hexafluoruro de azufre, el cual es usado como dieléctrico, es decir, como aislante en la electrónica. Otro compuesto de flúor que es utilizado como aislante eléctrico es el politetrafluoruroetileno, un polímero mejor conocido como teflón. Este materia es utilizado comúnmente en utensilios de cocina, como sartenes y ollas, debido a su capacidad de rozamiento baja y facilidad de limpieza.

Cloro
El uso más comercial del cloro es en su forma de hipoclorito de sodio, cuya disolución en agua es llamada lejía.

Este compuesto es utilizado abundantemente para eliminar las bacterias en las piscinas y en el agua potable. Asimismo se emplea en los desinfectantes y blanqueadores. De hecho el cloro es muy efectivo contra la bacteria Escherichia coli.

El cloruro de polivinilo o PVC y otros plásticos son obtenidos a partir del cloro. El PVC se emplea para elaborar ropa, pisos, tejas del techo, cables eléctricos, tubos flexibles, tuberías, estatuas, camas de agua y estructuras inflables.

Otro uso de este elemento es en la obtención de bromo a partir de las salmueras, mediante la oxidación del bromuro con cloro:
2Br – + Cl2 → Br2 + 2Cl-
Es necesario utilizar un proceso de destilación para separarlo del Cl2.
Otro compuesto de cloro que posee importancia comercial es el cloruro de metilo, el cual es empleado en medicina como anestésico. De igual manera, se usa para fabricar algunos polímeros de silicona y para extraer grasas, aceites y resinas.
El cloroformo, triclorometano o tricloruro de metilo, es un compuesto químico de fórmula química CHCl3 que puede obtenerse por cloración como derivado del metano o del alcohol etílico. Este compuesto se emplea como disolvente habitual en los laboratorios de química y biología, por ejemplo en la extracción de vitaminas y sabores. Entre otras aplicaciones del cloroformo es en la extracción y purificación de la penicilina y otros antibióticos. Además para la purificación de diversos alcaloides.
El tricloroetileno es otro compuesto de cloro de suma importancia, que se usa primordialmente como solvente para eliminar grasa de partes metálicas, sin embargo también es un componente en adhesivos, líquidos decapantes de pintura, para corregir escritura a máquina y quitamanchas.
En el pasado se empleaba con más frecuencia el gas cloro en las fuerzas armadas debido a que es un gas venenoso. En la actualidad es más utilizado por grupos terroristas.
Bromo.
El bromo y sus compuestos son empleados en la medicina, específicamente el bromuro de potasio, el cual fue empleado en el siglo 19 como anticonvulsivo. En la actualidad es solo utilizado en animales, debido a que causa disfunciones neurológicas en los seres humanos.
El bromo se emplea ampliamente en la elaboración de retardantes de llama. Funciona de la siguiente manera: cuando esta sustancia se quema, el bromo bloquea el fuego del oxígeno produciendo que este se extinga.
El bromuro que se obtiene del calcio, sodio y zinc se emplea para preparar soluciones específicas para la perforación de sal. También en la elaboración de aceites vegetales bromados que se emplean como emulsión en ciertas marcas de bebidas gaseosas.

En menor medida, el bromo se usa en el mantenimiento de piscinas, específicamente en baños termales. Asimismo, en la desinfección de aguas industriales, como antiséptico e insecticida.

En la industria textil es empleado en la fabricación de colorantes para telas.

Un compuesto importante del bromo es el bromuro de etilo, el cual es una sustancia tóxica usada como antidetonante en la gasolina, que al igual que el plomo previene la degradación del motor. La mezcla de plomo (tetraetilplomo) y bromo es sumamente tóxica, ya que genera un compuesto volátil llamado bromuro de plomo, el cual se escapa con los gases quemados hacia el ambiente, contaminándolo. Esta aplicación perdió interés económico desde la década de los años 70, debido a los problemas ambientales que generó.
Sin embargo, se ha retomado el uso del bromo en automóviles, pero en este caso en baterías para vehículos eléctricos para ayudar que estos no provoquen ningún tipo de emisiones.
Yodo.
El uso principal que presenta el yodo es en el campo de la medicina. Por ejemplo, las soluciones de yodo- alcohol y complejos de yodo se emplean como antisépticos y desinfectantes. De hecho una gran cantidad de productos de esterilización usados en el cuerpo contienen yodo, ya que es un eficaz limpiador para las heridas. Además es utilizado en forma de tabletas o en estado líquido para purificar el agua.

Por su parte, los isótopos radiactivos del yodo se aprovechan en la medicina nuclear y en otros campos como trazadores.
También es utilizado en la prevención del bocio, que es la inflamación del área de la garganta y la glándula de la tiroides. La insuficiencia de yodo es la causa más frecuente del bocio. El cuerpo requiere de yodo para producir la hormona tiroidea.
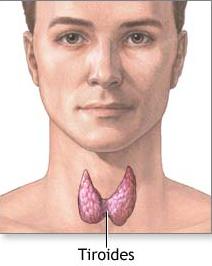
Además, el yodo también presenta aplicaciones del tipo no médicas como por ejemplo, en la elaboración de emulsiones fotográficas, preparación de tintes y lámparas halógenas.

Otro uso significativo es para originar la lluvia con la finalidad de obtener mejoras en el campo de la agricultura. Esto se logra utilizando el yoduro de plata dispersado en las nubes.
Ástato.
El ástato tiene 31 isótopos elevadamente inestables, por lo que solo se han podido producir unos pocos microgramos en los laboratorios. Por esta razón, no presenta alguna aplicabilidad comercial, salvo en investigaciones científicas y médicas.

Tennessine.
Al igual que muchos elementos radiactivos y sintéticos, al producirse en pequeñas cantidades, no posee uso comercial. Por lo tanto, es empleado en menor medida en la investigación científica.


