Los peróxidos son compuestos inorgánicos que presenta en su molécula un grupo peroxo, el cual consiste de la unión de dos átomos de oxígeno, cuyo estado de oxidación es -1.
La fórmula general de los peróxidos es: X2(O2)n
Donde:
X: elemento menos electronegativo que el oxígeno, generalmente metales.
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de míO: oxígeno
n: estado de oxidación del metal

Los peróxidos se pueden nombrar siguiendo las siguientes nomenclaturas:
Nomenclatura Sistemática IUPAC
Para nombrar compuestos bajo este sistema, se emplea prefijos griegos que indican la atomicidad de los elementos que conforman el compuesto.

Para los peróxidos se utiliza la siguiente fórmula:
prefijo (excepto mono)+peróxido+de+prefijo (excepto mono)+nombre del metal
Por ejemplo:
H2O2 Peróxido de dihidrógeno
Estequiométrica. Se nombra a los peróxidos de igual manera que los óxidos. Por ejemplo:
Na2O2 Dióxido de disodio
Nomenclatura Stock
Los peróxidos se nombran bajo este sistema, colocando el estado de oxidación del metal en números romanos, siguiendo la siguiente fórmula:
peróxido + de + metal + (estado de oxidación del metal)
Por ejemplo:
Fe2 (O2)3 Peróxido de hierro (III)
Nomenclatura Tradicional
Para nombrar compuestos bajo este sistema, es necesario seguir las siguientes reglas:
1. Cuando el elemento solo tiene una valencia, simplemente se coloca el nombre del elemento precedido de la sílaba “de” o bien se termina el nombre del elemento con el sufijo –ico.
2. Cuando el elemento tiene dos valencias diferentes se usan los sufijos -oso e -ico.
Oso: valencia menor
Ico: valencia mayor
3. Cuando el elemento tiene tres distintas valencias se usan los prefijos y sufijos: hipo-oso, oso, ico.
Hipo-oso: valencia menor
Oso: valencia intermedia
Ico: valencia mayor
4. Cuando el elemento posee cuatro valencias diferentes se usan los prefijos y sufijos: Hipo-oso, oso, ico, per-ico.
Hipo-oso: valencia menor
Oso: valencia media
Ico: valencia intermedia
Per-ico: valencia mayor
5. Si un elemento presenta 5 o más valencias diferentes, la última valencia sigue la nomenclatura Stock.
Por ejemplo:
El vanadio tiene 4 estados de oxidación diferentes: 2,3,4,5.
V2 (O2)5 Peróxido pervanádico
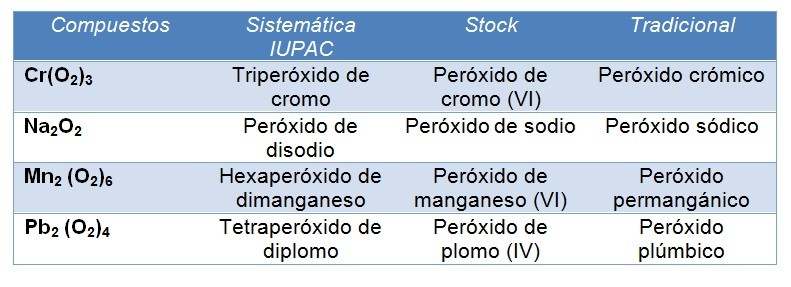
Otros ejemplos: