
En química, las moléculas no son planas, pero el papel y las pantallas sí lo son. Para resolver este dilema, los químicos inventaron diferentes «proyecciones». Cada una tiene un propósito específico: algunas sirven para ver rotaciones, otras para azúcares y otras para ciclos.
1. Proyección de Cuña y Enlace (3D Estándar)
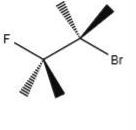
Es la forma más común de representar la estereoquímica.
- Características: Usa líneas normales para enlaces en el plano, cuñas rellenas para lo que sale hacia ti y cuñas discontinuas para lo que se aleja.
- Uso: Dibujo general de cualquier molécula orgánica.
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de mí2. Proyección de Newman
Imagina que miras la molécula directamente a lo largo de un enlace carbono-carbono.
- Características: El átomo delantero es un punto y el trasero es un círculo.
- Uso: Es perfecta para estudiar la estabilidad de los confórmeros (eclipsada vs. alternada) y las interacciones de torsión.

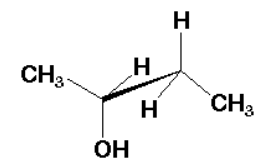
3. Proyección de Caballete (Sawhorse)
Es similar a la de Newman, pero vista desde un ángulo lateral oblicuo.
- Características: Muestra el enlace central como una línea larga diagonal.
- Uso: Útil para visualizar la orientación espacial de los grupos adyacentes sin perder la perspectiva del enlace central.
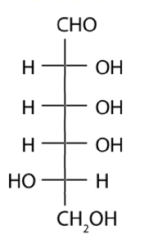
4. Proyección de Fischer
Representa moléculas quirales (como aminoácidos o azúcares) como una cruz.
- Características: Las líneas horizontales «salen» hacia ti y las verticales «se alejan».
- Uso: Estándar para determinar la configuración R/S en carbohidratos de forma rápida.
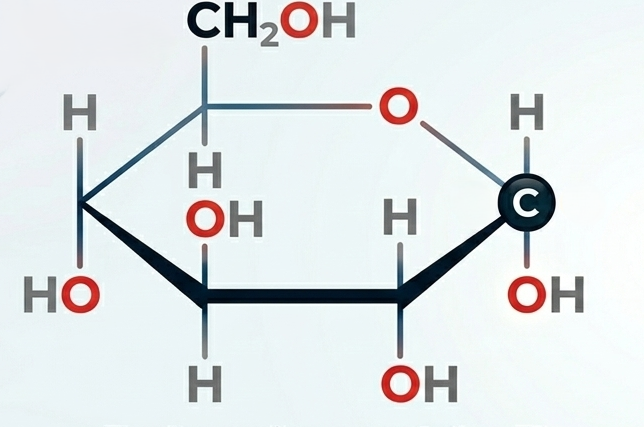
5. Proyección de Haworth
Es la forma clásica de representar azúcares en su forma cíclica (anillos).
- Características: El anillo se dibuja plano con un borde más grueso para indicar que está más cerca del observador.
- Uso: Identificar si un azúcar es alfa (α) o beta (β).
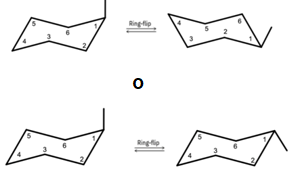
6. Proyección de Silla (Ciclohexano)
A diferencia de Haworth, esta muestra la verdadera forma tridimensional de los anillos de seis carbonos.
- Características: Diferencia claramente entre posiciones axiales (arriba/abajo) y ecuatoriales (hacia los lados).
- Uso: Determinar qué posición es más estable para sustituyentes voluminosos.
Similitudes y Diferencias
| Proyección | ¿Qué prioriza? | Similitud con otras | Diferencia principal |
| Newman | Rotación de enlaces | Comparte lógica con Caballete. | Vista frontal total («ojo en el eje»). |
| Fischer | Quiralidad y azúcares | Se parece a la Cuña en su lógica de profundidad. | Es una representación plana y rígida. |
| Silla | Estabilidad de anillos | Es la versión «realista» de Haworth. | Muestra ángulos de enlace reales (109.5°). |
| Caballete | Perspectiva 3D | Híbrido entre Cuña y Newman. | El enlace C-C es el protagonista visual. |
Resumen de similitudes
- Todas intentan representar la disposición espacial de los átomos para predecir reactividad.
- Cuña, Newman y Caballete suelen usarse para moléculas acíclicas (cadenas abiertas).
- Haworth y Silla son exclusivas para moléculas cíclicas.
Bibliografía Consultada
Para asegurar la precisión científica de este post, se han consultado las siguientes fuentes de referencia en química orgánica:
-
Wade, L. G., & Simek, J. W. (2017). Química Orgánica (9ª ed.). Pearson Educación. (Capítulos sobre Estereoquímica y Estructura de Alcanos).
-
McMurry, J. (2012). Química Orgánica (8ª ed.). Cengage Learning. (Secciones sobre Conformaciones de Cicloalcanos y Carbohidratos).
-
Clayden, J., Greeves, N., & Warren, S. (2012). Organic Chemistry (2nd ed.). Oxford University Press. (Capítulos detallados sobre Estereoquímica y Conformación).
-
IUPAC. Compendium of Chemical Terminology (The «Gold Book»). Projections. Recuperado de: https://goldbook.iupac.org/

