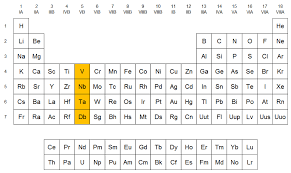
La familia del vanadio pertenece a los metales de transición y está conformado por los elementos: vanadio (V), niobio (Nb), tantalio (Ta) y dubnio (Db).
Este grupo posee en sus niveles electrónicos más externos cinco electrones de valencia, es decir, 2 electrones s de la última capa y 3 electrones d en la penúltima.
La estabilidad del estado de oxidación +5, el cual es el predominante en el grupo, va en aumento a medida que también aumenta el número atómico en combinaciones del tipo ácido.

¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de míPropiedades físicas
- Son sólidos a temperatura ambiente
- Son de color plateado y poseen brillo metálico
- Conducen calor y electricidad
- Presentan altos puntos de fusión y de ebullición

Propiedades químicas
- Predomina el estado de oxidación +4.
- Son bastante reactivos. La reactividad de estos elementos aumenta a medida que se desciende en el grupo.
- Son poco nobles, aunque al estar recubiertos por una capa superficial de óxido provoca una inercia química que es superada a altas temperaturas.
- Sólo producen complejos solubles con ácido fluorhídrico (HF).
- La fusión de sus óxidos con hidróxidos alcalinos origina vanadatos, niobatos y tantalatos.
- Forman compuestos de coordinación, esto debido a su facilidad para formar enlaces covalentes con la participación de electrones d y por su tendencia a reaccionar químicamente en diferentes estado de oxidación estables y a cambiar con relativa facilidad de unos estados de oxidación a otros.
Usos y aplicaciones de los elementos del grupo 5
Vanadio.
El principal uso de este metal de transición es en aleaciones como las de Vanadio-Níquel y Vanadio-Cromo, esto debido a que proporciona dureza y resistencia a la tensión. El acero originado por al aleación Vanadio-Cromo es ideal para la construcción de muelles, engranajes de transmisión y otras piezas de motores. Por su parte, el acero que surge de la aleación Vanadio-Titanio, es utilizado en los cascos de cohetes, alojamientos de los motores de aviones reactores y para los componentes de los reactores nucleares.

Este metal también es usado como catalizador en la elaboración de ácido sulfúrico (H2SO4), llegando a sustituir al platino.
Es usado como agente reductor y como agente oxidante para la elaboración de ácido maleico.
El vanadio se utiliza para originar un imán de superconductividad con un campo de 175,000 gauss.
Niobio.
El niobio es usado ampliamente en la aleación con el acero inoxidable, debido a que suministra mayor resistencia a la corrosión, especialmente a altas temperaturas.
El niobio en estado puro posee propiedades adecuados para ser usado como material de construcción para plantas de energía nuclear.
Este metal a estar aleado con el estaño, titanio o circonio, se emplea en la elaboración de súper-conductores y es un componente primordial en muchas súper-aleaciones.
Otro uso bastante popular e importante, es en la joyería.

Tantalio.
El tantalio al igual que los otros elementos que conforman este grupo, es usado principalmente en aleaciones ya que posee una gran resistencia a la corrosión, una gran ductilidad y un alto punto de fusión.
Este metal se emplea como filamento para evaporar metales como el aluminio; y en la elaboración de condensadores electrolíticos y piezas del horno de vacío.
El tantalio es usado como pieza de los equipamientos electrónicos de uso cotidiano como: teléfonos móviles, cámaras, relojes finos, entre otros.

Al ser muy versátil es usado ampliamente en las fuerzas militares, como armaduras de vehículos, explosivos y fabricación de misiles.
Al ser totalmente inerte en presencia de los líquidos corporales, el tantalio resulta de lo más útil, en la medicina, para la elaboración de prótesis humanas.
Dubnio.
Al igual que muchos elementos radiactivos y sintéticos, al producirse en pequeñas cantidades, no poseen uso comercial. Por lo tanto, es empleado en la investigación científica.


