Si la quiralidad es el estudio de la asimetría y las «manos» químicas, la aquiralidad es el estudio de la simetría, el balance y la superposición. En el mundo microscópico, entender qué moléculas no poseen actividad óptica es tan importante como identificar las que sí lo hacen.
¿Qué es la Aquiralidad?
Una molécula es aquiral si su imagen especular es superponible a sí misma. En términos simples: si tomas la molécula, la miras en un espejo y luego intentas colocar la imagen del espejo exactamente sobre la molécula original y encajan en todos sus puntos, entonces es aquiral.
A diferencia de las moléculas quirales (que no tienen simetría), las moléculas aquirales poseen al menos un elemento de simetría.
¡Haz amigos nuevos GRATIS! 🌍
¿Cansado de la rutina? Únete a la mejor plataforma gratuita para conocer gente y compartir tus aficiones en tu ciudad.
Descubrir planes cerca de míElementos de Simetría: La clave del éxito
Para identificar una molécula aquiral sin tener que construir modelos 3D, buscamos «elementos de simetría». Los dos más importantes son:
- Plano de Simetría (σ): Es un plano imaginario que atraviesa la molécula de modo que una mitad es el reflejo exacto de la otra. Si trazas este plano, la molécula se divide en dos partes especulares.
- Centro de Inversión (i): Un punto central a través del cual cada átomo puede ser proyectado hacia el lado opuesto y encontrar un átomo idéntico a una distancia igual.
El fenómeno de los Compuestos Meso
Uno de los puntos donde más estudiantes se confunden es con los compuestos meso.
Un compuesto meso es una molécula que contiene dos o más centros quirales (carbonos asimétricos), pero que, debido a su estructura interna, posee un plano de simetría. Esto hace que la rotación óptica de un centro quiral sea cancelada por el otro. Resultado: la molécula es aquiral.
Ejemplo clásico: El ácido tartárico en su forma meso. A pesar de tener carbonos unidos a cuatro grupos diferentes, la molécula como un todo es simétrica.
Ejercicios de Práctica
Para dominar la aquiralidad, nada mejor que la práctica. Analiza las siguientes moléculas y determina si son Aquirales o Quirales.
Ejercicio 1: Metano (CH4)
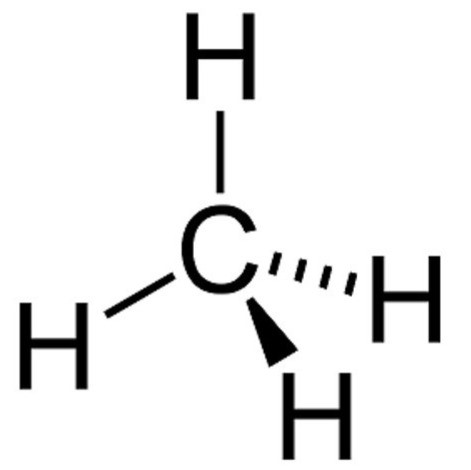
- Análisis: El carbono central está unido a cuatro átomos de hidrógeno.
- Pregunta: ¿Tiene un plano de simetría?
- Solución: Sí, tiene múltiples planos de simetría. Cualquier plano que pase por el átomo de carbono y dos de los hidrógenos dividirá a la molécula en dos mitades iguales.
- Conclusión: Es Aquiral.
Ejercicio 2: 1,1-diclorociclohexano
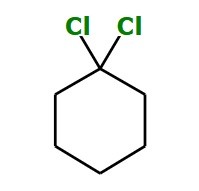
- Análisis: Observa el anillo de ciclohexano. En el carbono 1, tenemos dos átomos de cloro.
- Pregunta: Si pasamos un plano a través del carbono 1 y el carbono 4 del anillo, ¿qué sucede?
- Solución: Ese plano divide la molécula perfectamente por la mitad; el lado izquierdo del anillo es el reflejo del derecho.
- Conclusión: Es Aquiral.
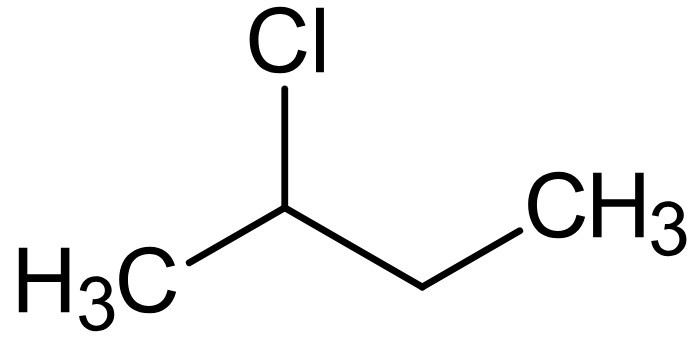
Ejercicio 3: 2-clorobutano
- Análisis: Carbono 2 unido a: -H, -Cl, -CH3, -CH2CH3.
- Pregunta: ¿Hay simetría?
- Solución: Los cuatro grupos son distintos. No existe ningún plano de simetría posible.
- Conclusión: Es Quiral.
Resumen
- Aquiral = Simetría. Siempre busca planos de simetría primero.
- No te fíes solo de los carbonos. Tener centros quirales no garantiza que la molécula sea quiral (recuerda los compuestos meso).
- La prueba de la superposición: Si puedes rotar la imagen especular y hacer que coincida, has encontrado una molécula aquiral.
La aquiralidad es la prueba de que en química, la ausencia de una propiedad (la quiralidad) es tan fundamental como su presencia. La simetría no es solo belleza; es una regla que define cómo interactúan las sustancias con la luz y con nuestro propio cuerpo.
Fuentes Consultadas
- McMurry, J. (2017). Química Orgánica (9na ed.). Cengage Learning.
- Carey, F. A., & Giuliano, R. M. (2017). Organic Chemistry (10th ed.). McGraw-Hill Education.
- Notas sobre Estereoquímica y Elementos de Simetría, Departamento de Química Orgánica.